Почему нельзя просто так взять, и соединить два металла? Болт представляет собой крепёжное изделие, изготовленное из металла. Во избежание ситуации, изображённой на картинке, в процессе эксплуатации он не должен корродировать и вызывать окисления того, что он крепит.

Причины разрушения крепежа
Из-за высокой цены и хрупкости, чистое железо, неспособное корродировать, не применяется в промышленности. Применяются сплавы, содержащие в себе примеси других металлов. А когда разные металлы контактируют в присутствии электролита, возникает гальваническая коррозия, которая разрушает изделие в короткие сроки.
К разрушению металла приводят все коррозионные процессы, при этом они имеют единую химическую сущность — окисление. Упрощённо окисление можно назвать процессом обмена веществ электронами. Окисляясь, одно вещество отдаёт электроны, а другое, восстанавливаясь, получает их. Для того чтобы понять суть коррозионного процесса, следует вспомнить об электрохимическом ряде напряжений (активности) металлов, в котором все металлы расположены слева направо в порядке повышения «благородности».

Более активные металлы находятся слева, справа расположены менее активные. Когда в контакт вступают металлы различной активности, они образуют гальваническую пару. В таких условиях для запуска процесса коррозии необходим лишь электролит, и отыскать его несложно. Это любая жидкость, которая проводит электричество. Из-за содержания минеральных веществ, даже простая вода из-под крана является отличным электролитом. Сюда же отнесите атмосферные осадки, банальный конденсат и т.п. Итак, в присутствии электролита более активный металл (анод) корродирует, а менее активный (катод) не подвергается коррозии. Указанные окислительно – восстановительные реакции – это основа всех коррозионных процессов. Разумеется, способность окисляться у разных металлов неодинакова, металлы, расположенные в ряду левее, более склонны отдавать электроны (а значит их способность к окислению выше), чем металлы, стоящие правее.
На деле описанный процесс происходит следующим образом. Например, стальной болт закрепили гайкой из меди. Железо, как более активный элемент (стоит левее), будет разрушаться в месте соединения. А если гайка изготовлена из алюминия, ситуация будет иной — уже алюминий, который является более активным металлом, будет разрушаться, теряя электроны. Суть приведенных примеров сводится к тому, что контакт более активных «левых» металлов с менее активными «правыми» усиливает коррозию первых.
Важно не допускать разрушения соединений, вследствие растворения крепежей. Ведь независимо от того, для чего служит соединение, последствия всегда неприятны. Грамотный подход к выбору материалов крепёжа, с учетом того, из чего изготовлены детали, поможет обеспечить достаточную износостойкость монтируемой конструкции.
Помните о нескольких основных правилах
- Не используйте соединения металлов, которые обладают большой разницей потенциалов. Из приведённой ниже таблицы следует, например, что крепеж, покрытый цинком, не следует применять на нержавеющей стали и алюминии. Использовать латунные винты опасно для крепления бронзовых деталей.
Материал детали
Крепеж
рекомендованный к использованию
недопустимый к использованию
Алюминий Нержавеющий Оцинкованный или латунный Оцинкованная сталь Оцинкованный или нержавеющий Латунный или бронзовый Бронза Бронзовый или нержавеющий Латунный Латунь Бронзовый или латунный Нержавеющий Нержавеющая сталь Нержавеющий или из монели Оцинкованный или латунный - Из другой таблицы, изображённой ниже, можно почерпнуть более детальную информацию о металлах, корродирующих в паре слишком быстро, и тех, что можно использовать в контакте. Таблица составлена в соответствии с требованиями межгосударственного стандарта ГОСТ 9.005–72, он закрепляет показатели единой системы защиты от коррозии и старения, а также определяет допустимые и недопустимые контакты с металлами и неметаллами.
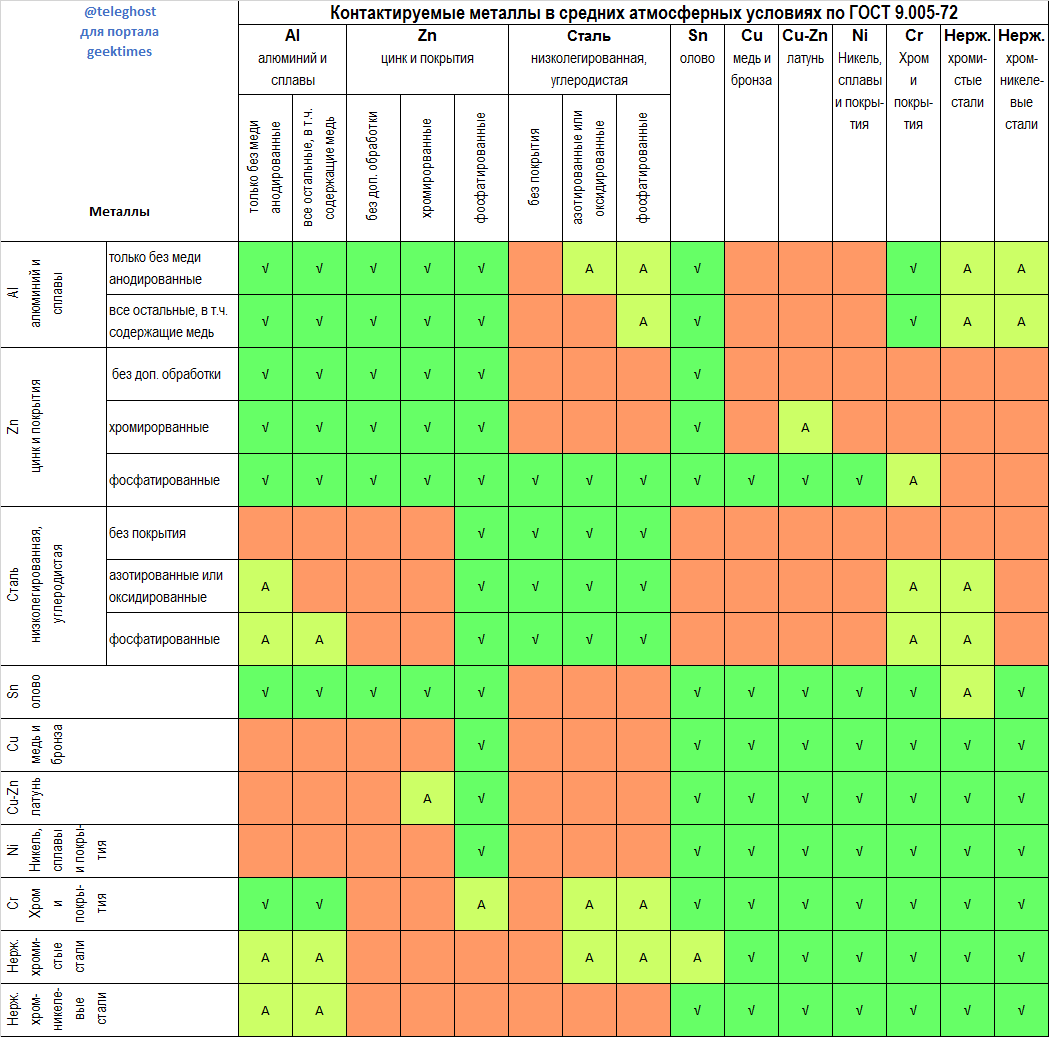
- При монтаже помните, что материал крепежа (анод) должен быть активнее материала конструкции (катода).
- Поверхность конструкции (катода) должна быть больше поверхности крепежа (анода).
- При монтаже соединения изолируйте металлы друг от друга, например, с помощью покрытия изолируйте их от электролита. При этом использование фум-ленты хорошо снижает электрический контакт и соответственно коррозию, чего нельзя сказать об анаэробном герметике, нити Tangit Uni-Lock или сантехническом лёне.
- Если соединение на воздухе, — старайтесь максимально защитить конструкции от действия влажности, таким образом вы исключите электролит из системы.
- Учитывайте, что агрессивная внешняя среда в виде щелочей, кислот, солей, газов и высокой температуры значительно ускоряют процесс коррозии.
Не пренебрегайте указанными правилами, внимательно изучайте материалы, из которых изготовлены детали, используйте данные приведенные в таблицах, – это поможет вам смонтировать действительно прочное соединение, которое прослужит длительное время, не создавая угрозы окружающим.




Добавить комментарий